Berikut ini admin akan memberikan informasi yang bermanfaat sekaigus untuk menambahkan pengetahuan anda di dalam ilmu laboratorium kimia, yaitu disini kita akan membahas metode analisis dengan Atomic Absorption Spectrophometri (AAS). Untuk melihat seperti apa contoh metode analisisnya silahkan anda perhatikan dan baca dengan baik pembahasannya berikut ini.
Langkah-langkah analisis dengan AAS
Peru anda ketahui berikut ini adalah langkah demi langkah untuk analisis dengan menggunakan metode Atomic Absorption Spectrophometri (AAS), berikut langkah-langkahnya:
- Menyiapkan larutan standar
- Preparasi sampel
- Memilih garis resonansi
- Optimasi kondisi alat
- Membaca absorbansi larutan standar
- Membaca absoransi larutan sampel
- Mengintrapolasi absorbansi larutan sampel pada kurva linier.
Kondisi untuk Analisis AAS
Untuk melakukan analaisis dengan menggunakan metode AAS berikut ini adalah beberapa Kondisi untuk analisisnnya yaitu sebagai berikut:
| Unsur | lmax (nm) | Tipe Nyala | Sensitivitas (µg/mL) | Range kerja(µg/mL) | Batas deteksi(µg/mL |
| Ag | 328,1 | AA | 0,029 | 1-5 | 0,002 |
| Au | 242,8 | AA | 0,11 | 5-20 | 0,009 |
| Bi | 223,1 | AA | 0,20 | 10-40 | 10-40 |
| Ca | 422,7 | NA | 0,013 | 1-4 | 0,002 |
| K | 766,5 | AP | 0,009 | 0,5-2 | 0,002 |
| Mo | 313,3 | NA | 0,28 | 15-60 | 0,03 |
| Sn | 224,6 | AH | 1,0 | 15-60 | 0,03 |
| Zn | 213,9 | AA | 0,009 | 0,4-1,6 | 0,001 |
| Zr | 360,1 | NA | 9,1 | 400-1600 | 1,0 |
Pembuatan Larutan Standar
Berikut adalah dimana larutan standar dibuat, untuk penjelsannya adalah sebagai berikut:
- Memperhitungkan konsentrasi larutan standar masuk dalam range linier
- Pembuatan larutan standar dapat dilakukan dengan cara pengenceran larutan induk dengan menggunakan labu takar pada volume tertentu.
- Deretan larutan standar minimal 3 varian, biasanya dibuat 5 varian.
Preparasi Sampel
Selanjutnya lanjut ke tahapan preparasi sampel, untuk lebih jelasnya adalah sebagai berikut:
- Sampel dapat berupa padat, cair dan gas.
- Agar dapat dianalisis dengan AAS, sampel harus berupa larutan jernih dan homogen boleh berupa larutan berwarna
- Sampel berupa oli, darah, serum, dll harus diencerkan dengan pelarut tertentu atau diabukan kemudian dilarutkan.
- Volume minimal sampel 0.5 mL
- Bebas dari matriks pengganggu
- Larutan dengan pelarut organik dapat dianalisis secara langsung jika viskositasnya tidak jauh berbeda dengan viskositas air.
- Pelarut tidak mengganggu nyala api, contoh CCl4 dapat memadamkan api udara-asetilen, penggunaan metilisobutil keton dan campuran hidrokarbon dapat meningkatkan pembentukan atom-atom gas pada keadaan GS sehingga dapat meningkatkan sensitifitas sampai 3x lipat daripada menggunakan pelarut air.
- Penggunaan pelarut kloroform dapat menimbulkan ledakan pada nyala sehingga harus dihindarkan penginjeksian secara langsung.
- Sisa-sisa asam pendestruksian juga harus diencerkan karena jika kosentarsi asam terlalu tinggi dapat menyebabkan korosi pada sistem pembakaran.
Destruksi Basah
Berikut ini adalah penjelasan mengenai destruksi basah diantaranya sebagai berikut:
- Destruksi basah adalah perombakan sampel dengan asam-asam kuat baik tunggal maupun campuran, kemudian dioksidasi dengan menggunakan zat oksidator.
- Pelarut-pelarut yang dapat digunakan untuk destruksi basah antara lain asam nitrat, asam sulfat, asam perklorat, dan asam klorida.
- Semua pelarut tersebut dapat digunakan baik tunggal maupun campuran.
Contoh cara destruksi basah
Berikut adalah contoh dari cara melakukan destruksi basah diantaranya sebagai berikut:
- Sebanyak 1 gram sampel sayuran dimasukkan ke dalam gelas beker 100 mL
- Ditambahkan larutan aqua regia atau campuran HNO3 pekat : HCl pekat (1:3) sebanyak 3 mL.
- Dipanaskan di atas hotplate selama kurang lebih 30 menit sampai tidak terbentuk gas.
- Setelah semua sampel terdestruksi dan terbentuk larutan kemudian disaring dan disimpan di dalam botol sampel.
- Diperoleh larutan sampel hasil destruksi basah siap dianalisis.
Destruksi Kering
Dan selanjutnya yaitu lanjut ke destruksi kering berikut adalah penjelasannya, diantaranya sebagai berikut:
- Destruksi kering merupakan perombakan organic logam di dalam sampel menjadi logam-logam anorganik dengan jalan pengabuan sampel dalam muffle furnace dan memerlukan suhu pemanasan tertentu.
- Pada umumnya dalam destruksi kering ini dibutuhkan suhu pemanasan antara 400-800oC, tetapi suhu ini sangat tergantung pada jenis sampel yang akan dianalisis.
Contoh cara destruksi kering
Tidak lupa juga dan berikut ini adalah beberapa contoh untuk cara melakukan destruksi kering, diantaranya sebagai berikut:
- Ditimbang sampel sebanyak 1 gram tempatkan pada cawan porselin.
- Diuapkan dengan oven sampai temperatr 105 – 110 oC selama 30menit.
- Diabukan didalam tanur selama 8 jam pada suhu 450 oC sampai sampel mengering.
- Sampel yang telah mejadi abu, kemudian ditambahkan HCl 10 M sebanyak 2 mL.
- Kemudian dipanaskan di atas hotplate sampai abu larut.
- Abu yang telah larut kemudian dipindahkan ke dalam labu takar 50 mL kemudian diencerkan dengan larutan HNO3 0,1 M sampai tanda batas.
- Larutan siap dianalisis.
Pemilihan garis resonansi
Berikut adalah langkah melakukan pemilihan garis resonasi, diantaranya sebagai berikut:
- Suatu unsur mempunyai banyak tingkat energi yang dapat digunakan untuk menyerap sinar.
- Contoh: Cu mempunyai 2 garis resonansi
Fe mempunyai 3 garis resonansi - Pada tabel alat dapat dilihat garis resonansi Cu yang peka, contoh:
| Garis resonansi | Konsentrasi | Absorbansi |
| 3247,5 | 0,01 mg/L | 0,01 |
| 2441,6 | 2441,6 | 0,01 |
Optimasi Kondisi Alat
Lanjut ke tahapan optimasi kondisi alat untuk penjelasannya lengkapnya sebagai berikut:
- Optimasi tinggi pembakar digunakan untuk mendapatkan populasi atom yang terbanyak sehingga pembakaran dapat tepat pada lintasan energinya.
- Optimasi laju alir gas pembakar dan oksidan berpengaruh pada suhu pengatoman. Jika gas pembakar kurang maka energi untuk pengatoman kurang sehingga pengatoman kurang sempurna, jika gas pembakar berlebih maka atom akan tereksitasi menjadi spesies bukan atom (M+ atau M*).
Metode Penentuan Konsentrasi
Berikut ini adalah metode penentuan konsentrasi, untuk melihat selengkapnya adalah sebagai berikut:
1. Metode Kurva Standar
Dilakukan dengan cara membandingkan absorbansi sampel terhadap kurva kalibrasi larutan standar (C vs Absorbansi).
Metode ini dilakukan jika:
- Konsentrasi sampel tidak terlalu kecil
- Preparasi mudah dilakukan
- Jumlah sampel banyak.
2. Metode Standar Adisi
Metode dengan menambahkan larutan standar ke dalam larutan sampel.
Metode ini perlu digunakan:
- Jika konsentrasi sampel sangat rendah, jika menggunakan metode kurva standar mempunyai resiko ketelitian rendah.
- Jika matrik dari sampel mempunyai gangguan yang besar terhadap analitnya.
- Sampel jumlahnya sedikit
Preparasi larutan untuk metode standar adisi
Berikut adalah Preparasi larutan untuk metode standar adisi untuk lebih jelasnya sebagai berikut:
| Labu takar | 1 | 2 | 3 | 4 | 5 |
| Vol. Sampel(mL) | 50 | 50 | 50 | 50 | 50 |
| Vol. Standar(10 mg/L), Ml | 0 | 2 | 4 | 6 | 10 |
| Vol. total | 100 | 100 | 100 | 100 | 100 |
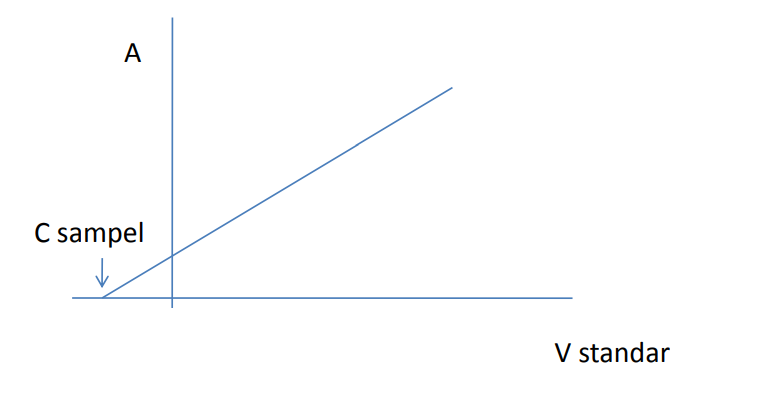
Interferensi dalam AAS
Berikut adalah beberapa interferensi dalam metode AAS diantaranya yaitu sebagai berikut:
1. Interferensi ionisasi
Terjadinya pembentukan ion M+ yang mengakibatkan menurunkan nilai absorbansi yang sebenarnya.
Penyebab: energi berlebihan
Cara mengatasi: dilakukan optimasi laju alir gas dan pembakar ulang.
2. Interferensi background
Terjadi karena terbentuknya oksida pada proses pengatoman.
Penyebab: penggunaan gas pembakar dan oksidan yang kurang tepat sehingga suhu pengatoman kurang efektif dan menyebabkan terjadinya oksida.
Cara Mengatasi: Tinjau ulang penggunaan pembakar dan oksidan.
3. Interferensi Spektral
Terjadi karena adanya overlaping absorpsi antara spesies penggangu dan spesies yang diukur karena rendahnya resolusi monokromator.
Misalnya: dua garis terletak berdekatan seprti Vanadium pada 308,211 nm dan alumunium pada 308,215 nm.
Cara mengatasi: memilih garis reonansi yang tidak berdekatan misal untuk Al dipilih garis resonansi pada 309,207 nm.
Untuk mengurangi interferensi spektra baik fotometri nyala maupun AAS adalah dengan meningkatkan resolusinya dengan menggunakan prisma dan filter, tetapi dengan keadaan tertentu untuk meningkatkan selektivitas hal tersebut dapat dihindari dengan teknik-teknik pemisahan sperti sistem penukar ion atau ekstraksi pelarut.
| Sumber Resonansi | Panjang Gelombang (nm) | Unsur yang dianalisis | Panjang gelombang (nm) |
| Aluminium | 308,211 | Vanadium | 308,216 |
| Antimon | 231,147 | Nikel | 231,147 |
| Tembaga | 324,754 | Europium | 324,754 |
| Galium | 403,307 | Magnesium | 403,307 |
| Besi | 271,903 | Platina | 271,903 |
| Raksa | 253,652 | Kobalt | 253,652 |
4. Interferensi kimia
Dapat terjadi karena terbentuknya senyawa yang stabil dan atau terjadinya ionisasi.
Contoh: adanya ion phospat dan sulfat dapat mereduksi atomisasi Ca. Al sebagai pengotor dapat mereduksi kecepatan atomisasi Mg.
A. Pembentukan Senyawa Stabil
- Terbentuknya senyawa stabil akan menyebabkan proses peruraian (disosiasi) tidak sempurna karena molekul-molekul stabil relatif sulit diuraikan menjadi atom-atomnya.
- Contoh: kasus penentuan kalsium dengan adanya sulfat atau phospat, terbentuknya oksida stabil dari unsur-unsur titanium, vanadium, dan aluminium.
Cara mengatasi terjadinya pembentukan senyawa stabil
- Meningkatkan temperatur nyala Peningkatan temperatur yang lebih tinggi akan menambah kemungkinan terbentuknya atom-atom gas bebas.
Contoh: alumunium oksida lebih cepat terdisosiasi dengan nyala nitrous oksidaasetilen karena mempunyai temperatur nyala lebih tinggi daripada nyala udara asetilen - Dengan menggunakan zat penukar *releasing agent) Reaksi umum : M-X + R ® R-X + M Dengan menambah zat pereaksi R akan meningkaatkan konsentrasi atom-atom gas logam M. Asumsi tersebut benar jika hasil enyawa R-X merupakan senyawa stabil.
Contoh: pada penentua Ca dengan adanya phospat, penambahan lantanum klorida atau stronsium klorida dalam larutan cuplikan akan terbentuk senyawa lantanum(stronsium) phospat dan selanjutnya Ca ditentukan dengan nyala udara asetilen tanpa adanya gangguan phospat lagi. Penambahan EDTA pada larutan cuplikan kalsium sebelum dianalisis mungkin dapat meingkatkan sensitivitas nyala karena terbentuk kompleks dengan EDTA yang lebih mudah terurai pada nyala api. - Ekstraksi logam Ekstraksi logam dapat digunakan untuk mengurangi efek interferensi. Ekstraksi akan memisahkan unsur-unsur yang menyebabkan interferensi dengan unsur analit. Zat analit yang sudah dipisahkan akan dapat ditentukan serapannya tanpa gangguan unsurunsur logam lain.
Contoh: pada penentuan tembaga dalam mineral batuan banyak mengandung besi, maka dapat diekstraksi dengan pengompleks asetilaseton dalam pelarut kloroform.
B. Terjadi ionisasi dalam keadaan GS
- Terbentuknya ion-ion logam dalam nyala api akan mengurangi emisi garis spektra atom pada spektroskopi emisi atau akan mengurangi besarnya absorpsi pada sistem AAS.
- Untuk mengurangi proses ionisasi ini dengan menggunakan temperatur nyala yang lebih rendah.
- Temperatur yang tinggi akan meningkatkan pembentukan ion-ion dari logam-logam alkali dan logam Ca, Sr dan Ba.
- Untuk mengurangi ionisasi dapat dilakukan dengan menambah zat penekan ionisasi. Zat ini biasanya merupakan larutan yang mengandung ion kalium konsentrasi 2000 ppm ditambahkan pada cuplikan Ca, Sr dan Ba.
- Air sadah dianalisis kandungan kalsiumnya dengan AAS pada 422,7 nm nyala nitrous oksidaasetilen. Pembacaan yang diperoleh: konsentrasi Ca(ppm)(absorbansi): 0(0); 1(0,090); 2,2(0,194); 3,10(0,273); 3,9(0,340); 5(0,440); 6(0,525). Jika sampel menunjukkan absorbansi 0,380, hitunglah konsentrasi Ca!
- Lima gram sampel kuningan dilarutkan dalam asam dan dibuat menjadi 500 mL. Analisis AAS untuk Zn pada 213,9 nm dengan menggunakan nyala udara-asetilendidapat hasil pembacaan sbb: ppm Zn(absorbansi): 0(0); 5(0,061); 10(0,122); 15(0,185); 20(0,248); 25(0,309); 30(0,370). Absorbansi sampel 0,164 hitunglah kadar Zn dalam sampel.
- Tuliskan cara membuat larutan standar Ag+ dari kristal AgNO3 dengan variasi konsentrasi 1,0; 1,5; 2,0; 2,5 dan 3,0 ppm masing-masing 10 mL. Larutan standar tersebut dibuat dari larutan induk 100 ppm.
- Mr AgNO3 = 169,8
- Ar Ag = 107,8
- 100 ppm = 100 mg dalam 1000 mL
- Berat Ag dalam AgNO3 = Ar Ag/Mr AgNO3 x berat AgNO3
- Fotometri nyala digunakan untuk analisis air sadah dalam penentuan konsentrasi Ca. Pembacaan skala yang diperoleh: [Ca](ppm)/Intensitas: (0/4), (2/9,6), (4/15,0), (6/20,0), (8/26,5), (10/31,9), (x/11,5) Hitunglah konsentrasi Ca dalam sampel yang dinyatakan dalam kesadahan CaCO3
- Sepuluh ml cuplikan air alam dipipet ke dalam 50 mL beberapa labu ukur. 0,00; 5,00; 10,00; 15,00 dan 20,00 mLlarutan standar yang mengandung 11,1 ppm Fe ditambahkan ke tiap larutan cuplikan,kemudian dilanjutkan penambahan ion tiosianat berlebih untukmenghasilkan kompleks merah Fe(SCN)2+ . Setelah pengenceran sampai tanda batas, absorbansi masing-masing larutan diukur dengan suatu fotometer yang dilengkapi filter hijau didapat absorbansi berturut-turut sbb: 0,215; 0,424; 0,685; 0,826 dan 0,967 (dengan sel 0,982 cm). Berapa konsentrasi Fe3+ dalam cuplikan air.
Itulah penjelasan yang dapat admin sampaikan kepada anda mengenai metode analisis dengan Atomic Absorption Spectrophometri (AAS), tidak lupa juga berikut kami menawarkan alat untuk AAS yang bisa anda lihat dibawah ini.
Jual alat AAS
Nah selain itu juga anda dapat melakukan pengukuran dengan menggunakan alat AAS yang bernama "(AAS) Atomic Absorption Spectrophotometer – AAS-120" dan disini kami menawarkan alat tersebut berikut.

1. Deskripsi alat AAS
AAS alat untuk menentukan kandungan logam dengan kategori logam berat dan logam ringan yang bernama (AAS) Atomic Absorption Spectrophotometer – AAS-120 dengan harga yang terjangkau dan kompettif berikut adalah keterangan alatnya.
(AAS) Atomic Absorption Spectrophotometer – AAS-120 AAS adalah alat yang digunakan untuk menentukan kandungan logam dengan kategori logam berat dan logam ringan. AAS yang dimiliki oleh laboratorium terintegrasi adalah AAS dengan merek Perkin Elmer Pinaacle 900T. AAS ini adalah salah satu alat yang paling canggih dan dapat digunakan untuk analisis dengan metode api atau tungku grafit. Gas yang digunakan adalah asetillin dan nitro oksida dengan kualitas UHP untuk menjamin kualitas hasil tes. Kadar logam yang dianalisis dapat berasal dari sampel air, tanah, makanan, kosmetik, obat -obatan, tanaman dan sebagainya. Jenis logam yang merupakan andalan pengujian adalah aluminium logam (AI), molibdenum (MO) dan silika (SI).
2. Fitur alat AAS
- Teknik analisis api udara-asetilen kaya oksigen yang inovatif
Teknik analisis nyala yang dipatenkan mengadopsi nyala api udara-asetilen yang kaya oksigen sebagai pengganti nyala nitro oksida-asetilen untuk analisis elemen suhu tinggi, seperti Ca, Al, Ba, W, Ti, V, dll. Suhu nyala terus menerus disesuaikan antara 2300 - 2950ºC, yang memungkinkan untuk memilih suhu atomisasi terbaik untuk elemen yang berbeda. Ini fitur pengoperasian yang mudah, biaya analisis rendah dan rentang analisis AAS bingkai lebar. Api oksigen yang kaya tidak akan mencemari lingkungan dan tidak berbahaya bagi tubuh manusia. Ini adalah terobosan dalam analisis AAS api. - Sistem atomisasi tungku api / grafit terintegrasi, dapat diubah dengan pembakar emisi api
- Pergantian yang dikontrol secara otomatis dari alat penyemprot api dan tungku grafit terintegrasi yang menampilkan pengoperasian yang mudah dan penghematan waktu
menghilangkan tenaga manusia. - Kepala pembakar emisi api dapat dipasang untuk melakukan analisis emisi api terhadap logam alkali seperti K, Na, dll.
- Pergantian yang dikontrol secara otomatis dari alat penyemprot api dan tungku grafit terintegrasi yang menampilkan pengoperasian yang mudah dan penghematan waktu
- Sistem kontrol otomatis yang akurat
- Turret 6 lampu otomatis, penyesuaian otomatis arus lampu dan optimalisasi posisi berkas cahaya.
- Pemindaian panjang gelombang otomatis dan pengambilan puncak.
- Spektral otomatis dan perubahan bandwidth.
- Pergantian otomatis antara operasi tungku api dan grafit, optimalisasi otomatis parameter posisi, pengaturan aliran gas otomatis.
- Analisis tungku grafit sepenuhnya otomatis yang andal
- Mengadopsi fuzzy-PID dan mode kurva ganda teknik kontrol suhu yang dikendalikan cahaya, teknik koreksi otomatis suhu, memastikan pemanasan cepat, reproduktifitas suhu yang baik, dan sensitivitas analitik yang tinggi. Akurasi kontrol suhu kurang dari 1%.
- Tungku grafit dengan kontrol pneumatik dan kunci tekanan, memastikan tekanan konstan dan kontak yang andal.
- Multi fungsi auto sampler menampilkan persiapan sampel standar otomatis, koreksi otomatis kedalaman probe pengambilan sampel, penelusuran otomatis dan koreksi ketinggian permukaan cairan di bejana sampler, dengan akurasi pengambilan sampel 1% dan reproduktifitas 0,3%, mewujudkan otomatisasi sepenuhnya analisis tungku grafit.
- Langkah-langkah perlindungan keamanan yang sempurna
- Alarm dan perlindungan otomatis terhadap kebocoran bahan bakar gas, aliran abnormal, tekanan udara yang tidak mencukupi dan pemadaman api yang tidak normal dalam sistem nyala api.
- Alarm dan fungsi perlindungan untuk gas pembawa dan tekanan gas pelindung yang tidak mencukupi, pasokan air pendingin yang tidak mencukupi dan pemanasan berlebih dalam sistem tungku grafit.
- Desain elektronik yang canggih dan andal
- Mengadopsi array logika skala besar yang dapat diprogram dan teknologi bus antar 12 C.
- Soket tipe Eropa dan AMPadapter dengan keandalan tinggi untuk memastikan keandalan jangka panjang dari keseluruhan sistem elektronik.
- Perangkat lunak analisis yang mudah dan praktis
- Perangkat lunak analisis AAS yang mudah digunakan dibuat di bawah Sistem Operasi Windows, mewujudkan pengaturan dan pengoptimalan parameter yang cepat.
- Pengenceran sampel otomatis, pemasangan kurva otomatis, koreksi sensitivitas otomatis.
- Perhitungan otomatis konsentrasi sampel (isi), nilai rata-rata, standar deviasi dan perhitungan standar deviasi relatif.
- Penentuan multi elemen secara berurutan untuk sampel yang sama.
- Data terukur dan hasil akhir dapat dicetak dan diedit dalam format Excel.
3. Comparison alat AAS
| Element | Wavelength (mm) | Rich oxygen air C2H2 flame | N2O-C2H2 flame | Air C2H2 flame |
| Ca | 422.7 | 0.009 | 0.05 | 0.07 |
| Yb | 378.8 | 0.037 | 0.08 | 7.6 |
| Eu | 459.4 | 0.137 | 0.3 | 3.0 |
| Al | 309.3 | 0.4 | 0.7 | |
| Sr | 460.7 | 0.016 | 0.1 | 0.15 |
| Ba | 553.5 | 0.1 | 0.4 | 10.0 |
| Mo | 313.3 | 0.15 | 0.4 | 0.8 |
| W | 255.1 | 3.2 | 5.0 | |
| Ga | 287.4 | 0.4 | 1.0 | 1.3 |
| Sm | 429.7 | 2.92 | 8.5 | |
| La | 550.1 | 37.2 | 35.0 | |
| Sn | 224.6 | 0.8 | 3.0 | 50 |
4. Spesifkasi alat AAS
| Main Specification | Wavelength range | 190-900nm |
| Wavelength accuracy | Better than ±0.25nm | |
| Resolution | Two spectral lines of Mn at 279.5nm and 279.8nm can be separated with the spectral bandwidth of 0.2nm and valley-peak energy ratio less than 30%. | |
| Baseline stability | 0.004A/30min | |
| Background correction | The D2 lamp background correction capability at 1Ais better than 30 times. | |
| The S-H background correction capability at 1.8Ais better than 30 times. | ||
| Light Source System | Lamp turret | Motorized 6-lamp turret (Two high performance HCLs can be mounted on the turret to increase the sensitivity in flame analysis.) |
| Lamp current adjustment | Wide pulse current: 0~25mA, | |
| Narrow pulse current: 0~10mA. | ||
| Lamp power supply mode | 400Hz square wave pulse; | |
| 100Hz narrow square wave pulse + 400Hz wide square pulse wave. | ||
| Optical System | Monochomator | Single beam, Czerny-Turner design grating monochromator. |
| Grating | 1800 l/mm | |
| Focal length | 277mm | |
| Blazed Wavelength | 250nm | |
| Spectral Bandwidth | 0.1nm, 0.2nm, 0.4nm, 1.2nm, auto switch over | |
| Flame Atomizer | Burner | 10cm single slot all-titanium burner. |
| Spray chamber | Corrosion resistant all-plastic spray chamber. | |
| Nebulizer | High efficiency glass nebulizer with metal sleeve, sucking up rate: 6-7mL/min | |
| Emission burner provided | ||
| Graphite Furnace | Burner | 10cm single slot all-titanium burner |
| Spray chamber | Corrosion resistant all-plastic spray chamber. | |
| Nebulizer | High efficiency glass nebulizer with metal sleeve, sucking up rate: 6-7mL/min. | |
| Emission burner provided | ||
| Graphite Furnace | Temperature range | Room temperature~3000ºC |
| Heating rate | 2000ºC/s | |
| Graphite tube dimensions | 28mm (L) x 8mm (OD) | |
| Characteristic mass | Cd≤0.8 ×10^12g, Cu≤5 ×10^12g, Mo≤1×10^12 g | |
| Precision | Cd≤3%, Cu≤3%, Mo≤4% | |
| Detection and Data | Detector | R928 photomultiplier with high sensitivity and wide spectral range. |
| Processing System | Software | Under Windows operating system |
| Analytical method | Working curve auto-fitting; standard addition method; automatic sensitivity correction; automatic calculation of concentration and content. | |
| Repeat times | 1~99 times, automatic calculation of mean value, standard deviation and relative standard deviation. | |
| Multi-task Functions | Sequential determination of multi-elements in the same sample. | |
| Condition reading | With model function | |
| Result printing | Measurement data and final analytical report printout, editing with Excel. | |
| Standard RS-232 serial port communication | ||
| Graphite Furnace Autosampler | Sample tray capacity | |
| Vessel material | Polypropylene | |
| Vessel volume | 3ml for sample vessel, 20ml for reagent vessel | |
| Minimum sampling volume | 1μl | |
| Repeatable sampling times | 1~99 times | |
| Sampling system | Accurate dual pump system, with 100μl and 1ml injectors | |
| Characteristic concentration and Detection Limit | Monochomator | Single beam, Czerny-Turner design grating monochromator |
| Grating | 1800 l/mm | |
| Focal length | 277mm | |
| Blazed Wavelength | 250nm | |
| Spectral Bandwidth | 0.1nm, 0.2nm, 0.4nm, 1.2nm, auto switch over | |
| Flame Atomizer | Air-C2H2 flame | Cu: Characteristic concentration ≤ 0.025 mg/L, Detection limit≤0.006mg/L; |
| Rich oxygen Air-C2H2 flame | Ba: Characteristic concentration ≤ 0.22mg/L | |
| Al: Characteristic concentration ≤ 0.4mg/L | ||
| Function Expansion | Hydride vapor generator can be connected for hydride analysis. | |
| Dimensions and Weight | Main unit | 107×49×58cm, 140kg |
| Graphite furnace | 42×42×46cm, 65kg | |
| Autosampler | 40×29×29cm, 15kg |
Nah itulah keterangan mengenai alat AAS yang kami tawarkan untuk anda, jika anda trtarik ingin membeli alat AAS Atomic Absorption Spectrophotometer tersebut, untuk melakukan pembeliannya anda silahkan hubungi kami melalui kontak yang tersedia di website ini atau dengan mengisi formulir penawaran dibawah ini untuk mengetahui harga AAS dan juga spesifikasi AAS secara lengkap.










